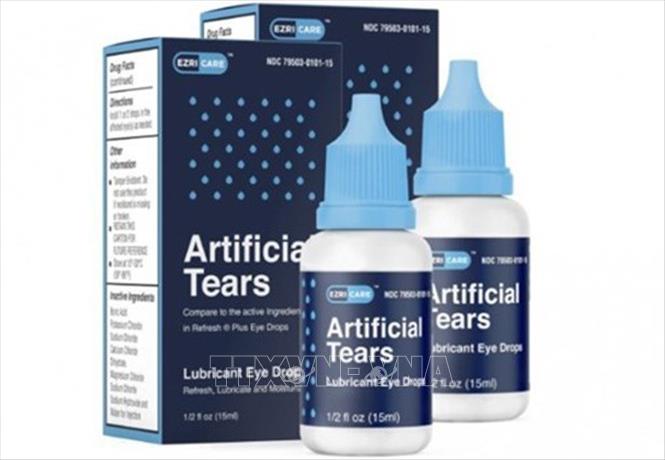
Nước mắt nhân tạo hiệu EzriCare. Ảnh: CNN/TTXVN
Nguồn tin của Bộ Y tế Ấn Độ khẳng định các xét nghiệm mà nước này tiến hành cho thấy các mẫu xét nghiệm sản phẩm thuốc nhỏ mắt Artificial Tears của công ty Global Pharma Healthcare đều đạt chuẩn. Thông tin trên được công bố gần 2 tháng sau khi cơ quan chức năng Mỹ cảnh báo nguy cơ sản phẩm đặc trị cho mắt này chứa vi khuẩn kháng thuốc.
Hiện người phát ngôn Bộ Y tế Ấn Độ và công ty Global Pharma Healthcare đều chưa đưa ra bất cứ bình luận nào trước thông tin trên.
Hồi tháng 2, Global Pharma Healthcare đã thông báo thu hồi tự nguyện trên toàn quốc sản phẩm Artificial Tears do nguy cơ nhiễm khuẩn. Cơ quan quản lý dược phẩm và thực phẩm (FDA) của Mỹ cho rằng Global Pharma Healthcare vi phạm quy định thực hành sản xuất tiêu chuẩn.
Trung tâm Kiểm soát và Phòng ngừa dịch bệnh (CDC) Mỹ đã xác định được sự hiện diện của "một chủng vi khuẩn hiếm gặp có khả năng kháng thuốc" ở 68 bệnh nhân ở 16 bang và hầu hết các trường hợp này đều báo cáo có sử dụng thuốc nhỏ mắt Artificial Tears tính đến ngày 14/3. Có ít nhất 3 người tử vong, và 8 ca báo cáo về mất thị lực, 4 trường hợp thông báo phải phẫn thuật cắt bỏ một nhãn cầu.
Ấn Độ là nước có ngành dược phẩm lớn thứ 3 thế giới. Tuy nhiên thời gian gần đây, hình ảnh nước này bị ảnh hưởng nghiêm trong sau vụ thuốc nhỏ mắt trên cùng sản phẩm siro ho được cho có liên quan đến ít nhất 70 trường hợp tử vong là trẻ em ở Gambia và 19 trẻ em ở Uzbekistan.